Как ярко демонстрирует практика, результаты интеллектуальной работы все чаще нуждаются в защите от злоумышленников, которые, прельстившись легким заработком, используют их в коммерческих целях. Как ни странно, пандемия подстегнула интерес к проблемам защиты патентов. «Пришпорила» она и законодательную инициативу в этой области. Раз уж мы вспомнили про коронавирус, то и разговор о защите результатов интеллектуальной деятельности у нас получится с легким привкусом медикаментов. На состоявшемся недавно вебинаре, посвященном особенностям защиты патентных прав, его участники обозначили проблемы в этой сфере и пути их решения на примере обращения лекарственных препаратов.
Центральное место в онлайн-дискуссии «Особенности защиты патентных прав в условиях пандемии и после», организованной Адвокатским бюро «Егоров, Пугинский, Афанасьев и партнеры», занял доклад Дмитрия Травникова, начальника управления организации и предоставления государственных услуг Роспатента. Он рассказал о работе органа в условиях пандемии и актуальных инициативах в области патентного права. Спикер обозначил проблемы защиты патентных прав при обращении лекарственных препаратов и подчеркнул важность создания нового механизма их защиты. Но обо всем по порядку.
Ни для кого не секрет, что интеллектуальная собственность становится для бизнеса главным активом, компании вкладывают миллиарды долларов в инновации, чтобы получить преимущество перед конкурентами. В настоящий момент весь мир трудится над созданием вакцины против коронавируса. При этом не все участники рынка хотят быть инноваторами, некоторые предпочитают воспользоваться плодами чужих интеллектуальных усилий, используют недобросовестные методы конкурентной борьбы. В таких условиях проблемы защиты патентных прав, интеллектуальных активов приобретают особое значение.
Пандемия свалилась как снег на голову
Дмитрий Травников отметил, что многие иностранные патентные ведомства во время пандемии перешли в режим онлайн-работы, некоторые из них в экстренном порядке приняли меры поддержки заявителей. Как ограничительные меры повлияли на режим работы Роспатента? Российское ведомство из общего тренда не выпало. Начал докладчик с рассказа о тех шагах, которые Роспатент, законодательная власть сделали навстречу заявителям, чтобы помочь в непростой ситуации. Конечно, в России, как это часто бывает с временами года, пандемия пришла неожиданно, и отчасти не все были к этому готовы. Самые жесткие ограничения начались «внезапно» для многих заявителей, и патентное ведомство было вынуждено подстраиваться под новые условия работы. Безусловно, эти ограничения имели сильное влияние на разные стороны деятельности компаний. В первую очередь компании начали испытывать затруднения в коммуникации с ведомством, а у многих были открыты незавершенные делопроизводства. В рамках этих делопроизводств необходимо было представлять в Роспатент документы, сроки актуальности которых были ограничены. Поэтому правительством и Госдумой был принят ряд инициатив, направленных на то, чтобы облегчить и без того непростое положение заявителей. В частности, был принят Федеральный закон от 01.04.2020 № 98-ФЗ «О внесении изменений в отдельные законодательные акты Российской Федерации по вопросам предупреждения и ликвидации чрезвычайных ситуаций», который касался самых разных сфер жизни, в том числе и сроков совершения заявителем, правообладателем и иным лицом действий, связанных с уплатой патентных и иных пошлин, необходимых для осуществления федеральным органом исполнительной власти по интеллектуальной собственности юридически значимых действий.
Позднее было принято постановление Правительства РФ от 20.06.2020 № 893 «О продлении сроков совершения заявителем, правообладателем и иным лицом действий, в том числе связанных с уплатой патентных и иных пошлин, необходимых для осуществления федеральным органом исполнительной власти по интеллектуальной собственности юридически значимых действий», вступившее в силу с 22 июня 2020 г. Оно предполагало, что те сроки, которые истекали или истекают в период с 30 марта по 30 ноября, будут продлены при наличии соответствующего ходатайства. Этим же постановлением был установлен срок подачи такого ходатайства — один месяц с даты вступления в силу постановления или с даты истечения установленного срока, который заявитель просил продлить, в зависимости того, какой из этих сроков истекал скорее. Все сроки продлеваются до 31 декабря.
Какие сроки могут быть продлены? По большому счету перечень сроков достаточно широк. Это сроки ответа на запросы ведомства, представления позиций в ответ на уведомления о результатах проверки патентоспособности, сроки результатов проверки соответствия заявленного обозначения. Были продлены и сроки уплаты разнообразных пошлин: за совершение юридически значимых действий, за продление срока действия охраны документов и т.д. То есть это все те сроки, которые вынужден, обязан соблюдать заявитель в ходе взаимодействия с Роспатентом. При этом в отношении действий самого ведомства сроки, установленные нормативно-правовыми актами, административным регламентом в том числе, остались без изменений.
Почему до 31 декабря? Учитывалось, что ограничения будут постепенно сниматься, в тот момент, когда вступало в силу постановление, уже снимались ограничения и ответные действия на пандемию становились более прозрачными и простыми. Но разработчики нормативного акта понимали, что за время пандемии, за время жестких ограничений, в организациях накопилось столько проблем, что их нужно решать постепенно и, к сожалению, не всегда вопрос правильного распоряжения интеллектуальной собственностью имеет для менеджмента первостепенное значение. Поэтому Роспатент посчитал правильным дать бизнесу возможность разгрести накопившиеся проблемы и отложить вопросы защиты интеллектуальных прав до конца года.
Кроме того, и это тоже довольно распространенный в мировой практике шаг, Роспатент ускорил рассмотрение заявок на изобретения для тех отраслей, которые оказались на «передовой» в сложившейся ситуации. Речь идет о заявках, которые касаются противовирусных лекарственных препаратов, средств диагностики, медицинских изделий, в том числе средств индивидуальной защиты. В рамках этой программы патентное ведомство рассматривало поступавшие заявки без взимания дополнительной платы в течение двух месяцев, не более.
Ведомство перешло на удаленку
Еще одним шагом стало расширение спектра действий в рамках электронного взаимодействия Роспатента и заявителей. К тем вызовам, с которыми мы столкнулись, Роспатент во многом оказался готовым именно в силу того, что по всем оказываемым услугам уже имелась возможность электронной подачи заявок. Пожалуй, единственным препятствием для более широкого использования электронных инструментов явилось то, что не у всех заявителей — физических лиц имеется в наличии усиленная квалифицированная электронная подпись.
Один из наиболее часто встречающихся вопросов, которые слышат органы Роспатента: нужно ли обоснование просьбы о продлении срока, подтверждающие документы и т.п.? Нет, ни указания причины продления сроков, ни подтверждающих документов предъявлять не нужно. Более того, подобное ходатайство составляется в произвольной форме и не требует уплаты пошлины. На его основании срок просто будет продлен до 31 декабря.
Роспатент пошел даже на беспрецедентный шаг, разрешив по некоторым услугам подавать запрос об их предоставлении по электронной почте. Это послабление в период самых жестких ограничений, когда были закрыты пункты приема физических документов, коснулось даже заявок на изобретение. Сейчас, впрочем, это уже не актуально, но этот опыт следует иметь в виду, если ситуация с ограничениями повторится.
Отдельно отметим, что в пандемийный период Роспатент сумел организовать удаленную работу своих экспертов. Во время самых жестких ограничений большая часть экспертов работала из дома. Для государственного служащего это, конечно, интересный опыт. Докладчик отметил, что ориентир на электронное взаимодействие, взятый Роспатентом некоторое время назад, оказался в итоге совершенно правильным. Случись коронавирус еще пять лет назад, ведомство, конечно, не было бы готово к форс-мажору. Сегодня же восемь из десяти заявок обрабатываются в «цифре», и уже можно с уверенностью говорить, что этот процесс адаптирован к самым невероятным, казалось бы, сценариям.
Единый реестр как защита всех участников оборота
В последние месяцы в полный рост встала проблема защиты патентных прав в отношении лекарственных препаратов. В связи с этим очень кстати созрела инициатива о создании единого Евразийского реестра фармакологически активных действующих веществ, охраняемых патентом на изобретение. Проблема тут заключается в следующем. Регистрация воспроизведенных аналогов лекарственных препаратов осуществляется Минздравом вне зависимости от действующих исключительных прав. Ведь Минздрав проверяет только эффективность и безопасность лекарственного препарата. Регистрация происходит задолго до истечения срока действия патента на изобретение, относящееся к оригинальному лекарственному препарату. Его последующее введение в гражданский оборот происходит до завершения действия патентных прав.
Судебные споры, не в упрек судебной системе будет сказано, рассматриваются долго. Сами по себе разбирательства, касающиеся защиты патентных прав на лекарственные препараты, сложны по своей сути и трудны с точки зрения судей, потому что для их рассмотрения требуется наличие специальных знаний, навыков. И рядовой судья не может их разрешить самостоятельно, он вынужден назначать экспертизу. Экспертные же заключения зачастую либо противоречат друг другу, либо как минимум содержат разные данные, а судье необходимо отдать предпочтение какому-либо одному из них. Это занимает время.
Все эти нюансы позволяют вывести лекарственный препарат на рынок в нарушение патентных прав, реализовать их пациентам. А когда препараты введены в гражданский оборот, ни один судья не заберет у пациентов лекарство. Длительное судебное рассмотрение спора позволяет компании-производителю воспроизведенного лекарственного препарата с нарушением патентных прав участвовать в аукционах, получать значительную прибыль в ущерб интересам компании-разработчика. Специалисты Роспатента считают существующие правовые механизмы недостаточно эффективными. Поэтому было предложено создать Евразийский реестр фармакологически активных действующих веществ, охраняемых патентом на изобретение (далее — Фармреестр).
Создание такого реестра позволит обеспечить учет действующих исключительных прав при регистрации лекарственного препарата. Реестр может также выполнять информационную функцию, он позволит оперативно получить информацию, непосредственно относящуюся к лекарственным препаратам, в которых используется соответствующее действующее вещество. И наконец, реестр позволит устанавливать дату вступления в силу регистрационного удостоверения с учетом прекращения действия патента.
Помимо этого, Фармреестр несет и прикладную функцию. Не в каждом из судебных процессов будет необходимость назначать дорогостоящие судебные экспертизы, любому судье будет понятно, что если в отношении препарата действует исключительное право, значит, его использование в лекарственном средстве допустимо только с согласия правообладателя.
Кроме того, Фармреестр можно будет использовать в рамках государственных закупок. Если на торгах предлагается лекарственный препарат, включающий в себя действующее вещество из Фармреестра, госорган, производящий закупку, должен будет понимать, что осуществлять производство препарата и реализацию программ закупки можно будет только с разрешения соответствующего правообладателя.
Каков предположительный характер функционирования Фармреестра? В Минздраве можно будет устанавливать дату вступления в силу регистрационного удостоверения с учетом наличия действующих исключительных прав. То есть регистрационное удостоверение будет выдаваться даже при наличии действующих исключительных прав, но оно будет вступать в силу, как предлагается, на следующий день после истечения действия патента.
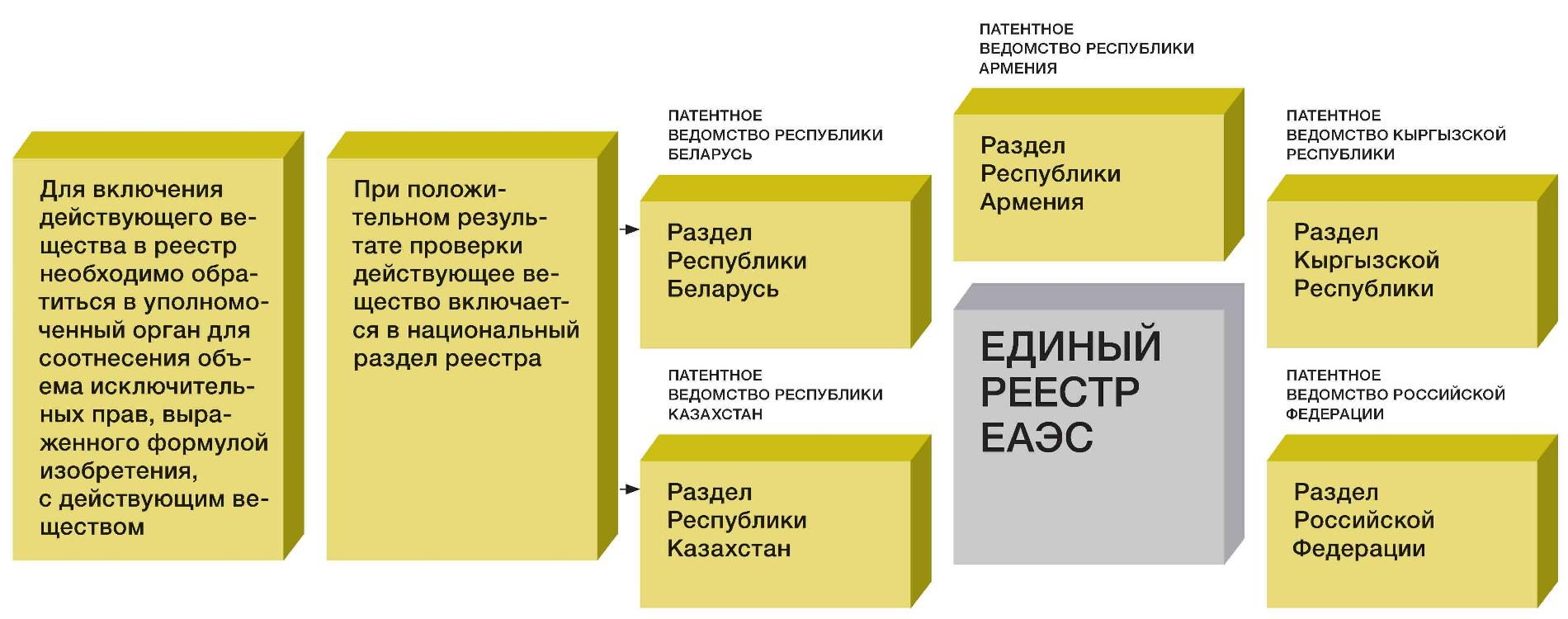
С 1 января 2021 г. регистрация лекарственных препаратов будет осуществляться по единым правилам Евразийского союза. Российское национальное законодательство в этой сфере перестает действовать, поэтому Роспатент предлагает предусмотреть то регулирование, которое будет действовать на территории всех пяти государств, входящих в ЕврАзЭС. Идея Роспатента заключается в том, чтобы единый реестр состоял, скажем так, из «национальных» разделов, формируемых национальными же уполномоченными ведомствами. Национальный минздрав в рамках процедуры регистрации лекарственного препарата будет учитывать те права, которые содержатся в каждом из национальных разделов. Заявитель, заинтересованное лицо, правообладатель смогут подать заявление в уполномоченные органы государства — члена Союза, те проведут проверочные мероприятия, распространяются ли на действующее вещество патентные права, и при положительном результате внесут соответствующие сведения в Фармреестр. Другие национальные минздравы будут учитывать вышеуказанные сведения в рамках процедур по выдаче регистрационного удостоверения либо признанию регистрационного удостоверения, выданного в другой стране.
Каковы реальные перспективы Евразийского Фармреестра? Представитель Роспатента признал, что его появление — вопрос даже не завтрашнего дня. Технически и кадрово патентные ведомства готовы к началу ведения Фармреестра, есть все необходимые предпосылки для появления соответствующего программного обеспечения. Минздравы смогут им пользоваться сразу же после того, как определенные изменения будут внесены в нормативно-правовую базу Евразийского экономического союза. Однако переговорный процесс между, казалось бы, заинтересованными сторонами проходит очень сложно. Партнеры российской стороны, в первую очередь минздравы, не разделяют уверенности Роспатента в необходимости ведения совместного реестра. И не желают проводить дополнительные проверки в ходе регистрации лекарственных препаратов. Защита патентных прав не входит в объем тех проверок, который минздравы привыкли проводить в рамках регистрационных процедур, осуществляемых сегодня.
Не реестром единым...
Какие есть еще инициативы в области защиты интеллектуальной собственности? Российская Федерация продолжает принимать те решения, которые способствуют переходу на полное электронное взаимодействие. Недавно президентом был подписан Федеральный закон «О внесении изменений в часть четвертую Гражданского кодекса РФ», который предполагает возможность предоставления совместно с заявкой трехмерных моделей заявляемых объектов интеллектуальной собственности. Это будет касаться изобретений, полезных моделей и промышленных и товарных образцов. Этот закон выгоден всем: он выгоден заявителям, которые начинают разработку своих технических решений в программах 3D-моделирования (не нужно будет переводить то, что создано в этой программе, в двумерный вид для того, чтобы подать заявку), эксперты смогут до мельчайших деталей получить представление о заявляемом техническом решении, что повысит качество и увеличит скорость экспертиз. А общество сможет лучше уяснить объемы правоохраны в связи с наглядным представлением объекта.
В планах Роспатента — создание системы, которая позволит в автоматическом режиме сравнить заявляемые модели с уже содержащимися в реестре.
Еще одним нововведением в этом же законе является выдача электронных охранных документов (сейчас патенты выдаются в бумажном «формате»). Это позволит после вступления закона в силу полностью перейти на электронное взаимодействие в рамках представления государственных услуг Роспатента. При этом пошлина за выдачу электронного патента будет отменена, в то время как за бумажное свидетельство ее придется заплатить. Таким образом ведомство планирует стимулировать интерес правообладателей к «цифре».
Еще одна инициатива — создание системы предварительного информационного поиска и предварительной оценки патентоспособности. Предполагается, что с помощью этой системы заявитель перед началом экспертизы по существу сможет обратиться в аккредитованную Роспатентом научную образовательную организацию для того, чтобы она по заявке провела предварительно информационный поиск и дала предварительную оценку патентоспособности. Технологии развиваются очень быстро, сейчас появляются такие сферы, в которых сложно разобраться даже эксперту. Да и содержать армию экспертов по всем областям науки и техники не может позволить себе ни одна страна мира. Поэтому зачастую заявки рассматриваются экспертами из смежных областей или даже теми, которые в данный момент оказались под рукой. Ну и, кроме того, надо заметить, что отнюдь не эксперты находятся на переднем крае науки и техники. Науку двигают именно научные и образовательные организации, там лучше знают, что же происходит в конкретной области техники, какие результаты демонстрируют специалисты в конкретных областях.
По замыслу Роспатента, данная новация позволит сократить сроки получения патента, повысит его надежность и создаст конкурентный рынок услуг по поиску и оценке патентоспособности.
Алгоритм принятия решения регистрации лекарственного препарата
|
Наличие действующего вещества в национальном разделе евразийского реестра |
Наличие у заявителя права использования изобретения |
Решение |
|
Вещества нет |
- |
|
|
Вещество есть |
У заявителя есть право использования изобретения |
|
|
Вещество есть |
У заявителя нет права использования изобретения |
|
Процедура включения действующего вещества в евразийский реестр